
NEURALGIA DEL TRIGÉMINO - ¿ES POSIBLE TRATARLA CON TERAPIA MANUAL?
Katarzyna Wachowska
Fisioterapeuta
¿QUE ES LA NEURALGIA DEL TRIGÉMINO?
La NEURALGIA DEL TRIGÉMINO define una disfunción del nervio trigémino causada por una lesión del nervio en su recorrido entre la periferia y el Sistema Nervioso Central (SNC). El trigémino es el nervio que transmite la información sensorial de DOLOR, TEMPERATURA, TACTO y PROPIOCEPCIÓN de la cara, boca y cavidad nasal, además de inervar los músculos de la masticación (1,2).
La neuralgia del trigémino se caracteriza por ser un dolor espontáneo similar a las descargas eléctricas, intermitente y a menudo incapacitante con ataques que duran unos pocos segundos pero pueden persistir durante 1 a 2 minutos. Pocas veces ocurre durante la noche y generalmente afecta a la parte inferior de la cara. En algunos pacientes el dolor puede ser desencadenado por las actividades cotidianas como hablar, masticar, afeitarse, beber líquidos calientes o fríos, o cualquier contacto facial o la estimulación sensorial de la cara. Los síntomas del dolor pueden ser clasificados como disestesia, alodínia o hiperalgesia (2,3).
Se ha observado también que la neuralgia del trigémino se asocia frecuentemente con la disfunción temporomandibular y la alteración de los maseteros, lo que puede conllevar a una disminución de la amplitud de movimiento mandibular y/o un desplazamiento del contacto oclusal de los pacientes (4,5).
Según diferentes estudios epidemiológicos la neuralgia del trigémino es el tipo de dolor facial más frecuente con una prevalencia de 4-13 casos por 100.000 habitantes. Afecta en general a personas mayores de 50 años y con una frecuencia moderadamente superior en las mujeres con una proporción de 3: 2 (6,7).
La IHS (International Headache Society) clasifica la neuralgia del trigémino en dos categorías: idiopática y sintomática. La neuralgia del trigémino se denomina idiopática o clásica cuando se debe a:
- Compresión neurovascular, causada por un vaso sanguíneo en la zona de entrada del nervio en el tronco cerebral (3). Los microtraumatismos repetitivos vinculados a la pulsación vascular pueden inducir una desmielinización de las fibras y una posterior remielinización anómala con la creación de neoreceptores responsables del dolor (8).
- Lesión a nivel de las ramas periféricas. Las causas más frecuentes de la lesión periférica del trigémino incluyen traumatismos faciales, aplicación de anestesia local en la región de la cara, extracción dental (particularmente la eliminación de los terceros molares inferiores donde hay una proximidad anatómica con el nervio), colocación de implantes o tratamiento del canal. En neuralgia del trigémino de origen odontológico el dolor se presenta frecuentemente como intraoral con puntos gatillos alrededor de los dientes. Esto lleva a menudo a un diagnóstico erróneo y la realización de un tratamiento dental innecesariamente. Aunque la mayoría de las lesiones periféricas son reversibles, los casos más persistentes pueden afectar negativamente la calidad de vida del paciente (9,10).
La clasificación sintomática o secundaria se reserva a los casos cuando se han identificado otras enfermedades como:
- Enfermedades neurológicas como la esclerosis múltiple, síndrome de Sjögren, enfermedad de Hansen (lepra), trastornos autoinmunes que causan inflamación del nervio o infección por herpes zóster.
- Lesiones craneales y médulares o tumores intracraneales que comprimen el nervio afectando su función.
- Deformidad del cráneo o compresiones en la fosa posterior (2,3).
En el caso de la neuralgia sintomática del examen neurológico puede mostrar deterioro sensorial en la distribución del nervio trigémino que es atribuible a la lesión subyacente (11,12).
En el diagnóstico de la neuralgia del trigémino la historia clínica tiene una importancia capital (2). Para evaluar las diferentes funciones del sistema trigeminal las pruebas sensoriales y motoras son imprescindibles en el examen clínico. Estas deberían incluir pruebas de sensibilidad cutánea (tacto, dolor y temperatura), pruebas de función motora y exploración de los reflejos. Además, la función del trigémino debe examinarse en el contexto de sus tres divisiones neurológicas (13). La resonancia magnética es actualmente la prueba de imagen más utilizada para descartar causas como la compresión del trigémino por malformaciones vasculares o tumores (3).
LOS TRATAMIENTOS ACTUALES DE LA NEURALGIA DEL TRIGÉMINO
Los estudios actuales muestran que el abordaje más utilizado para tratar el dolor en neuralgia del trigémino es el tratamiento farmacológico. Según la publicación de la Academia Americana de Neurología (AAN) y Federación Europea de Sociedades Neurológicas (EFNS) del año 2008 las drogas antiepilépticas carbamazepina y oxcarbazepina se utilizan como terapia de primera línea para controlar el dolor. La segunda línea de terapia incluye lamotrigina, el baclofeno y tratamientos alternativos como la toxina botulínica de tipo A.
Aunque la mayoría de los pacientes responde bien al tratamiento farmacológico, este presenta muchos efectos secundarios como sedación, mareos, náuseas, la ataxia y riesgos por el hígado y sistema hematológico por lo que puede ser contraindicado para pacientes de edad avanzada. La intervención quirúrgica suele reservarse para pacientes que no responden favorablemente al tratamiento médico o cuando los medicamentos están causando efectos adversos inaceptables (3).
La aplicación de la terapia manual para el tratamiento de la neuralgia del trigémino es muy escasa y la evidencia actual se limita al análisis de casos individuales. Los estudios como el de Rodine et al (12) o estudio de Grgic (14) muestran que la aplicación de terapia manual cervical y de ATM ha sido muy eficaz para controlar el dolor de los pacientes con neuralgia del trigémino sin el uso de los medicamentos. Sin embargo, en la actualidad, siguen siendo pocas las evidencias de la eficacia clínica de la terapia manual, por lo que es necesario realizar más investigaciones de calidad.
¿POR QUE TERAPIA MANUAL CERVICAL?
Para considerar la terapia manual cervical para tratar la neuralgia del trigémino tenemos que ver cuál es la relación del nervio trigémino con los cervicales. Por eso reseguiremos brevemente el recorrido del nervio trigémino.
Desde las 3 ramas periféricas del trigémino: oftálmica, maxilar y mandibular los impulsos eléctricos se dirigen al ganglio del trigémino que contiene los cuerpos celulares de casi todas las fibras sensoriales del trigémino (2,3). Desde el ganglio del trigémino los procesos centrales de las células neurales siguen la raíz sensorial del trigémino y entran en la porción lateral de la protuberancia del tronco del encéfalo para terminar en el largo NÚCLEO SENSITIVO (3). Aquí conectan con las neuronas de segundo orden que transmiten la información a los centros superiores (15) (Figura 1).
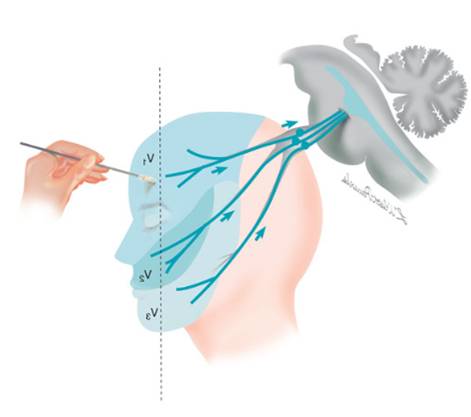
Figura 1. Via sensitiva del trigémino: ramas periféricas - oftálmica, maxilar y mandibular, ganglio del trigémino, raíz sensorial, nucleo sensitivo. (Cranial Nerves Illustrated [Internet]. Linda Wilson-Pauwels 2013 [consulta el 22 d’Abril de 2017]. Disponible a: https://bmc.med.utoronto.ca/cranialnerves/illustrations-by-chapter/trigeminal-v).
El núcleo sensitivo del trigémino se divide en 3 partes (Figura 2):
- la parte más craneal, núcleo mesencefálico, donde acabarán principalmente las fibras de propiocepción;
- en medio, núcleo sensorial principal, donde acabarán principalmente las fibras del tacto;
- la parte más caudal, núcleo del tracto espinal, donde acabarán las fibras del dolor y temperatura. En los mamíferos el núcleo del tracto espinal se subdivide en 3 subnúcleos: oral, interpolares y caudalis.

Figura 2. A. F. propioceptivas de los músculos extraoculares; B. F. táctiles y de presión de la zona oftálmica; C. F. de dolor y temperatura de la zona oftálmica; D. F. táctiles y de presión de la zona maxilar; E. F. de dolor y temperatura de la zona maxilar; F. F. táctiles y de presión de la zona mandibular; H. F. de dolor y temperatura de la zona mandibular; I. F. propioceptivas de los músculos de la masticación. (Liu GT. The Trigeminal Nerve and Its Central Connections [Internet]. Neuro-Ophthalmology Virtual Education Library (NOVEL): Walsh and Hoyt’s Clinical Neuro-Ophthalmology, 6th Edition. 2005 [cited 2016 Nov 13]. p. 1233–51. Available from: http://content.lib.utah.edu/cdm/singleitem/collection/EHSL-NOVEL/id/1570).
El núcleo del tracto espinal recibe la información de todas las ramas del trigémino (13) y se extiende por la médula hasta el nivel C2-C3. En este nivel las neuronas del asta dorsal de los segmentos cervicales superiores y el núcleo del tracto espinal del nervio trigémino no están separados por una línea definida sino definen una sola columna de la materia gris donde las neuronas de la cabeza, cara, cuello y del área cervical superior convergen y comunican. Este espacio se conoce como el NÚCLEO TRIGEMINOCERVICAL (12).
La convergencia de estímulos dolorosos en este nivel provoca un aumento de la función sináptica dentro del SNC que se traduce en una disminución del umbral de las neuronas convergentes dando lugar a una sensibilización central.
Una vez activada, esta facilitación central puede permanecer autónoma por un tiempo, o sólo requiere un nivel muy bajo de entrada de los nociceptores para sostenerla. Esto se traduce en una excitabilidad del circuito central y una activación de las respuestas de dolor exageradas y prolongadas. En consecuencia, el dolor podría convertirse en una percepción ilusoria que se produce en ausencia de estímulo nociceptivo y ser determinado por el estado de excitabilidad de las neuronas en el SNC (4).
Otro factor que puede contribuir al mantenimiento de la sensibilización central son los cambios en las células inmunes del SNC - microglia y astrocitos. En procesos nociceptivos normales estas poblaciones de células actúan proporcionando vigilancia inmune y mantenimiento de la homeostasis metabólica del SNC. En cambio, en presencia de un daño del sistema nervioso central o periférico se vuelven altamente reactivas y liberan mediadores para inducir y/o mantener la hiperexcitabilidad del SNC y la nocicepción anormal (15).
El estudio en animales conducido por Lee at al (15) demostró que la lesión del nervio periférico desencadena reacciones de las microglia y astrocitos dentro del SNC. Tras la ligadura del nervio mentoniano en ratas los micrògila y astrocitos mostraron signos de activación y cambios morfológicos significativos en el complejo nuclear del trigémino, especialmente en el núcleo principal sensorial y el subnúcleo caudalis donde terminan las fibras nociceptivas primarias (Figura 3 y 4). El incremento de activación más significativo de los microglia se observó entre el día 3 y 14 posterior a la lesión mientras que la actividad de astrocitos comenzó 14 días después de la lesión y se mantuvo elevada al menos hasta 28 días.
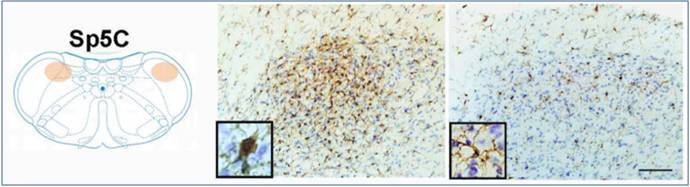
Figura 3. Reacción MICROGLIAL en respuesta a la lesión del nervio mentoniano 14 días posteriores a la lesión. La inmunotinción por Iba-1 en subnuclio caudalis (Sp5C). Augmento significativo en inmunoreactividad de Iba-1 en ratas con lesión neural junto con cambios notables en la forma de la celula microglial (izquierda) comparado con controles (derecha) (Lee S, Zhao YQ, Ribeiro-Da-Silva A, Zhang J. Distinctive response of CNS glial cells in oro-facial pain associated with injury, infection and inflammation. Mol Pain. 2010; 6:79).
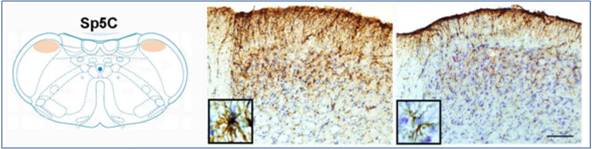
Figura 4. Reacción de los ASTROCITOS en respuesta a la lesión del nervio mentoniano 14 días posteriores a la lesión. La inmunotinción por GFAP en subnuclio caudalis (Sp5C). Augmento en inmunoreactividad de GFAP en ratas con lesión neutal junto con los cambios notables en la forma celular de astrocitos (izquierda) comparado con controles (derecha) (Lee S, Zhao YQ, Ribeiro-Da-Silva A, Zhang J. Distinctive response of CNS glial cells in oro-facial pain associated with injury, infection and inflammation. Mol Pain. 2010; 6:79).
La evidencia de sensibilización a nivel del núcleo caudalis en neuralgia del trigémino invita a preguntar si la terapia manual de la región cervical alta podría inhibir la activación central y en consecuencia reducir el dolor del trigémino. Los diferentes estudios muestran que la fuerza mecánica del la terapia manual inicia una cascada de respuestas neurofisiológicas del sistema nervioso periférico y central que resultan en hipoalgesia y cambios en la actividad simpática (16).
La primera teoría más aceptada fue la de "GATE CONTROL" de Melzack y Wall que afirma que la entrada no nociceptiva suprime la salida dolorosa mediante la inhibición de los nociceptores del asta dorsal. Este mecanismo se desencadena por tacto o la información sensorial no amenazadora activando fibras Aβ que inhiben la entrada nociceptiva de fibras aferentes Aδ y C (17).
Actualmente sin embargo el mecanismo más aceptado por el que la terapia manual induce la analgesia es a través de los CIRCUITOS DESCENDIENTES desde el mesencéfalo hacia el asta dorsal médular mediante la liberación de neurotransmisores. Estas sustancias como la serotonina, oxitocina, los endocannabinoides y los opioides endógenos actúan modulando los circuitos nociceptivos y percepción del dolor, siendo estos últimos los péptidos que tienen un efecto analgésico 18 a 33 veces más potente que la morfina (17).
Por lo tanto, aunque no se puede esperar resolver completamente la neuralgia del trigémino con técnicas manuales, sería lícito considerarlas para atenuar el dolor, mejorar la calidad de vida de los pacientes y probablemente disminuir el uso de los fármacos.
REFERENCIAS BIBLIOGRÁFICAS
1. Tortora GJ, Derrickson B. Principios de Anatomía y Fisiología. 11ª ed. Madrid: Editorial Médica Panamericana; 2006.
2. Royden Jones, Jr H. Netter’s Neurology. Elsevier; 2005.
3. Mahtani AA, Sethu G. Review on Trigeminal Neuralgia. Journal of Pharmaceutical Sciences and Research. 2016; 8(6):570-74.
4. Woolf CJ. Central Sensitization: Implications for the diagnosis and treatment of pain. Pain. 2011; 152(3):1–31.
5. Westersund CD, Scholten J, Turner RJ. Relationship between craniocervical orientation and center of force of occlusion in adults. Cranio [Internet]. 2016; Available from: http://dx.doi.org/10.1080/08869634.2016.1235254.
6. Seijo F. Neuralgia del trigémino. Rev Soc Esp Dolor. 1998; 5:70–8.
7. Bescós A, Pascual V, Escosa-Bagé M, Màlaga X. Tratamiento de la neuralgia del trigémino: actualización y perspectivas futuras de las técnicas percutáneas. Rev Neurol. 2015; 61(3):114–24.
8. Leclercq D, Thiebaut J-B, Héran F. Trigeminal neuralgia. Diagn Interv Imaging. 2013; 94:993–1001.
9. Zakrzewska JM. Multi-dimensionality of chronic pain of the oral cavity and face. J Headache Pain. 2013; 14:37.
10. Peñarrocha M, Peñarrocha D, Bagán J V, Peñarrocha M. Post-traumatic trigeminal neuropathy. A study of 63 cases. Med Oral Patol Oral Cir Bucal. 2012; 17(2):297–300.
11. Al-Quliti KW. Update on neuropathic pain treatment for trigeminal neuralgia. The pharmacological and surgical options. Neurosciences. 2015; 20(2):107–14.
12. Rodine RJ, Aker P. Trigeminal neuralgia and chiropractic care: a case report. J Can Chiropr Assoc. 2010; 54(3):177–86.
13. Liu GT. The Trigeminal Nerve and Its Central Connections [Internet]. Neuro-Ophthalmology Virtual Education Library (NOVEL): Walsh and Hoyt’s Clinical Neuro-Ophthalmology, 6th Edition. 2005 [cited 2016 Nov 13]. p. 1233–51. Available from: http://content.lib.utah.edu/cdm/singleitem/collection/EHSL-NOVEL/id/1570.
14. Grgic V. Influence of manual therapy of cervical spine on typical trigeminal neuralgia: a case report. Lijecnicki vjesnik. 2010; 132:21–4.
15. Lee S, Zhao YQ, Ribeiro-Da-Silva A, Zhang J. Distinctive response of CNS glial cells in oro-facial pain associated with injury, infection and inflammation. Mol Pain. 2010; 6:79.
16. Bialosky JE, Bishop MD, Price DD, Robinson ME, George SZ. The Mechanisms of Manual Therapy in the Treatment of Musculoskeletal Pain: A Comprehensive Model. Man Ther. 2009; 14(5):531–8.
17. Vigotsky AD, Bruhns RP. The Role of Descending Modulation in Manual Therapy and Its Analgesic Implications: A Narrative Review. Pain Res Treat. 2015.
Últimos artículos
- CRANIOFACIAL DISORDER ACADEMY
7 Mayo, 2021 - DOLOR LUMBAR CRÓNICO INESPECÍFICO BASADO EN LA SENSIBILIZACIÓN CENTRAL Y EFECTOS TERAPÉUTICOS DE LA TERAPIA MANUAL
20 Diciembre, 2019 - OCLUSIÓN, POSTURA, CONTROL MOTOR, DOLOR Y SUS RELACIONES CON LA DISFUNCIÓN MANDIBULAR
28 Octubre, 2018 - ¿QUÉ ES LA DISMENORREA Y COMO SE TRATA?
23 Mayo, 2018 - ENTENDER EL DOLOR
31 Enero, 2018
